Non serve essere esperti in ambito medico per capire che la tecnologia sta prendendo piede anche in questo settore, come in moltissimi altri, coadiuvando il lavoro umano e rendendolo più preciso.
Un insieme di migliorie importanti è rappresentato dai software medicali, degli applicativi progettati per agevolare le operazioni sanitarie che spaziano dalla gestione clinica della diagnosi del paziente fino al trattamento indicato. Sviluppati per soddisfare esigenze mediche specifiche, questi strumenti seguono normative precise e garantiscono la salute dei pazienti.
Cosa si intende per medical device?
Un software medicale può essere di diverso tipo: da una semplice applicazione fino al un gestionale complesso. I sistemi ospedalieri vengono progettati per ottimizzare il lavoro all’interno delle strutture, integrando vari moduli (gestione cartelle elettroniche, programmazione di appuntamenti, gestione delle risorse umane, fatturazioni, inventario dei farmaci).
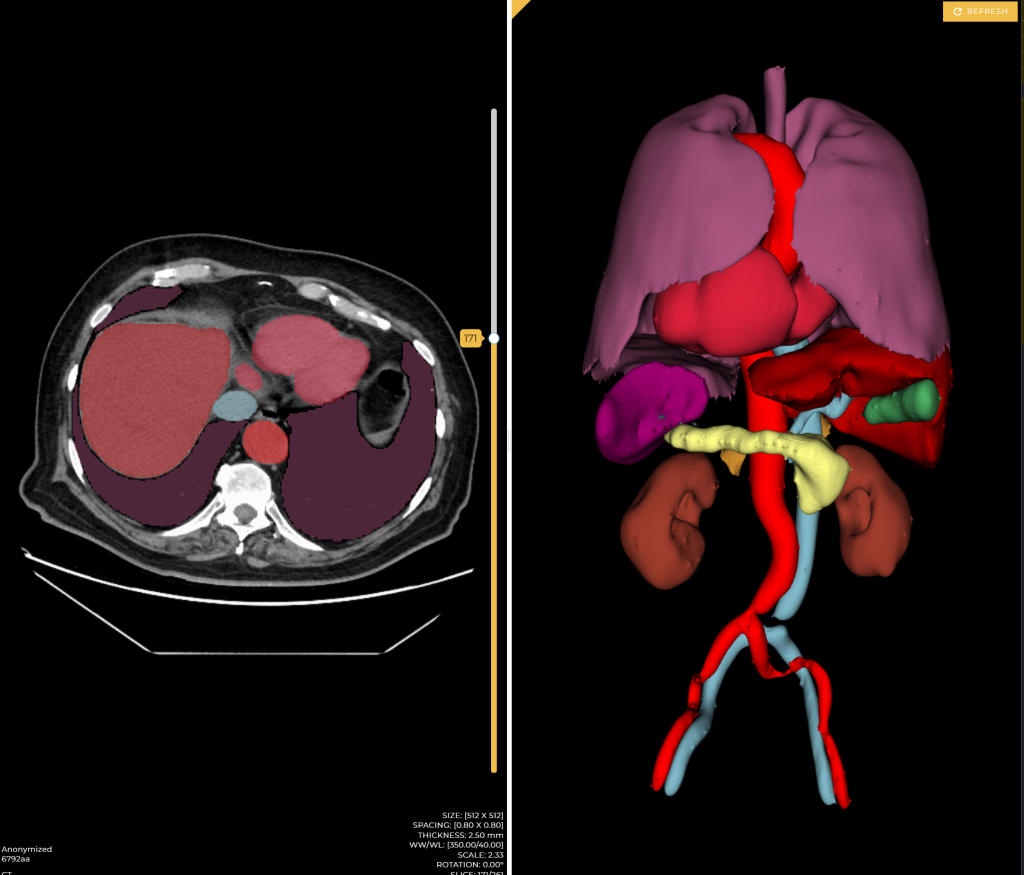
Chiamati anche HMS, tali gestionali riducono gli errori e migliorano la comunicazione fra i reparti, ma possiamo considerare medical device anche un sistema di diagnostica e imaging come la risonanza magnetica, la tomografia computerizzata, la radiografia e gli ultrasuoni. Con questi ausili, i professionisti identificano eventuali disturbi o patologie in modo accurato.
Ancora, sono software medicali le app di telemedicina, quelli di gestione della terapia e quelli di ricerca clinica per la raccolta dei dati di ricerca.
Quando un software deve essere considerato dispositivo medico?
Un software medicale, per essere tale deve avere uno scopo medico, quindi funzionalità complete che devono essere indicate nelle indicazioni fornite dall’azienda fabbricante.
Oltre a questa prima caratteristica, ci sono altri fattori che determinano la classificazione: il software deve controllare un dispositivo medico, fornire informazioni decisionali immediate e garantire supporto agli operatori sanitari.
Regole per la classificazione del software medicale
Con l’integrazione della tecnologia e il supporto dell’intelligenza artificiale, l’intero sistema ospedaliero si sta digitalizzando sempre di più: l’attività diagnostica e l’assistenza ai pazienti diventano migliori e si sviluppano così le Digital Therapeutics.
Il dispositivo medico veniva concepito, fino a questo momento, come semplice accessorio, ma è chiaro che non è più così. Adesso invece ci sono rigide regole a cui questi sistemi devono sottostare, per ottenere la certificazione software medicale.
Le modifiche in materia, si trovano in una guida emanata nel 2019, che aiuta i fabbricanti a individuare quando un software da loro realizzato deve essere inserito nel mercato oppure messo in servizio nel rispetto del Regolamento (UE) 745/2017 e, altresì, a determinare l’esatta categoria di rischio, appunto la classificazione.
Il software che fa funzionare un dispositivo, o comunque ne influenza l’uso, rientra nella stessa classe. Se il dispositivo non è destinato a essere usato principalmente in una determinata parte del corpo, viene classificato in base all’utilizzo più critico.
Al contrario, se un device non è connesso a nessun altro apparecchio, verrà classificato separatamente.
Vengono considerati anche i livelli di rischio, ovvero l’impatto che le informazioni fornite hanno sulla salute del paziente, in combinazione con la sua situazione patologica. Insomma, ci sono vari aspetti da considerare.
Certificazione del software medicale
Per certificare un software medicale, il produttore deve seguire un preciso processo che parte proprio dalla comprensione di un aspetto: il dispositivo è di tipo medico? La guida cui abbiamo accennato nel paragrafo precedente – pubblicata dal gruppo di coordinamento dei dispositivi medici della Commissione Europea – è utile a tale scopo e consultabile in qualsiasi momento; si trova infatti sul sito ufficiale.
Il produttore deve definire le modalità d’uso dello strumento e il meccanismo d’azione, per capire se questo rientra nella categoria. Dopo aver stabilito in quale classe rientra il dispositivo, si segue l’iter di conformità, che porterà poi all’ottenimento del marchio CE.
La certificazione software medicale richiede azioni e documentazione differenti in base alla classe e si va dalla semplice dichiarazione ad opera del fabbricante, fino a valutazioni complesse da parte di organismi notificati.
Innovazioni e tendenze future
Senza alcun dubbio, la disciplina del medical device è fra le più impattanti del MDR. La digitalizzazione della sanità, il cui primo passo è stato fatto per fronteggiare il Covid, è una realtà evidente e i benefici sono diversi, in termini di riduzione dei costi operativi, velocità e precisione. Dunque, il settore richiede attenzione e capacità.
Nell’ottica dello sviluppo di un software medicale di qualità, affidarsi a professionisti competenti è il primo passo per ottenere un buon prodotto.
D/Vision Lab: innovazione tecnologica per la sanità del futuro
Con un’esperienza approfondita nell’assistenza a professionisti di vari settori e nell’integrazione di sistemi avanzati con intelligenza artificiale, D/Vision Lab si posiziona come il partner ideale per sviluppare soluzioni software che migliorano la precisione, l’efficienza e la sicurezza delle cure sanitarie.